La Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) autorizó el uso de la vacuna de Pfizer/BioNTech contra el coronavirus para chicos de entre 12 y 15 años, permitiendo así ampliar la campaña de vacunación en ese país.
"La medida es un paso importante en la lucha contra la pandemia de covid-19", sostuvo la jefa interina de la FDA Janet Woodcock en un comunicado.
Desde diciembre de 2020, las vacunas de Pfizer habían sido aprobadas por la FDA para su uso en adultos y adolescentes de hasta 16 años. "Este es un momento decisivo en nuestra capacidad para combatir la pandemia del covid-19", dijo el pediatra y vicepresidente senior de Pfizer Bill Gruber.
La vacuna de Pfizer se está utilizando en varios países para adolescentes de hasta 16 años, y Canadá se convirtió recientemente en el primero en ampliar su uso a 12 años o más.
"Los padres y tutores pueden estar seguros de que la agencia llevó a cabo una revisión rigurosa y exhaustiva de todos los datos disponibles, como hemos hecho con todas nuestras autorizaciones de uso de emergencia de la vacuna covid-19", enfatizó Woodcock.
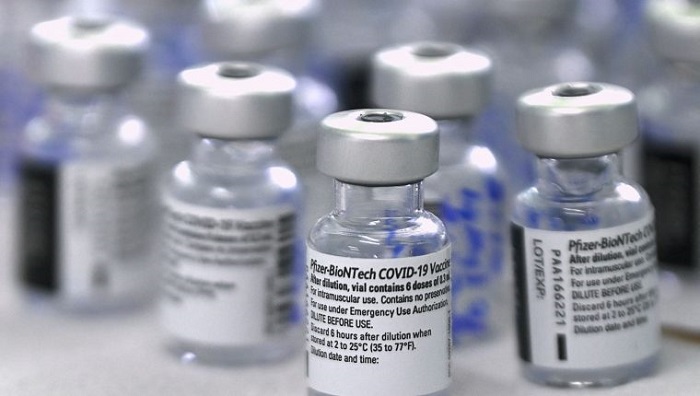
Si bien unas 260 millones de personas han sido vacunadas en Estados Unidos, las autoridades buscan incentivar a la población en medio de una disminución de la demanda.
La decisión de autorizar la vacuna se tomó tras un ensayo clínico realizado por Pfizer y BioNTech, en el que participaron 2.260 niños de entre 12 y 15 años que recibieron dos dosis de la vacuna o un placebo.
Durante la evaluación se registraron 18 casos de contagios en el grupo que recibió el placebo, mientras que no hubo ninguno en el conformado por los niños que recibieron la fórmula contra el virus. Otro dato alentador que encontraron los investigadores es que los niños desarrollaron niveles más altos de anticuerpos que los adultos jóvenes.
Entre marzo de 2020 y abril de 2021, en EE.UU. fueron detectados aproximadamente 1,5 millones de casos de covid-19 en adolescentes de entre 11 y 17 años.
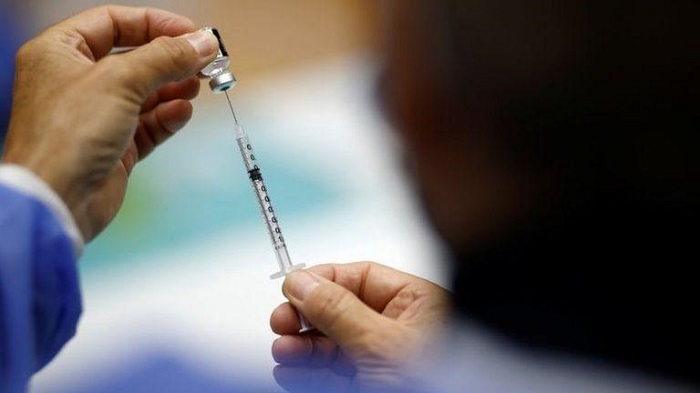
Con el visto bueno de la FDA, la farmacéutica solo necesita la habilitación de los Centros de Control y Prevención de Enfermedades (CDC), que revisará los datos en breve, para comenzar con la aplicación en la población.
Por otro lado, tanto Pfizer como Moderna han comenzado estudios en los EE.UU en niños de 6 meses a 11 años, con la finalidad de evaluar si los bebés, niños en edad preescolar y de primaria necesitarán dosis diferentes a las de los adolescentes y los adultos.
En tanto, AstraZeneca estudia la aplicación de su vacuna entre jóvenes de 6 a 17 años en Gran Bretaña, y en China Sinovac anunció recientemente que presentó datos preliminares a los reguladores nacionales que muestran que su vacuna es segura en niños de hasta tres años.